脳梗塞とは
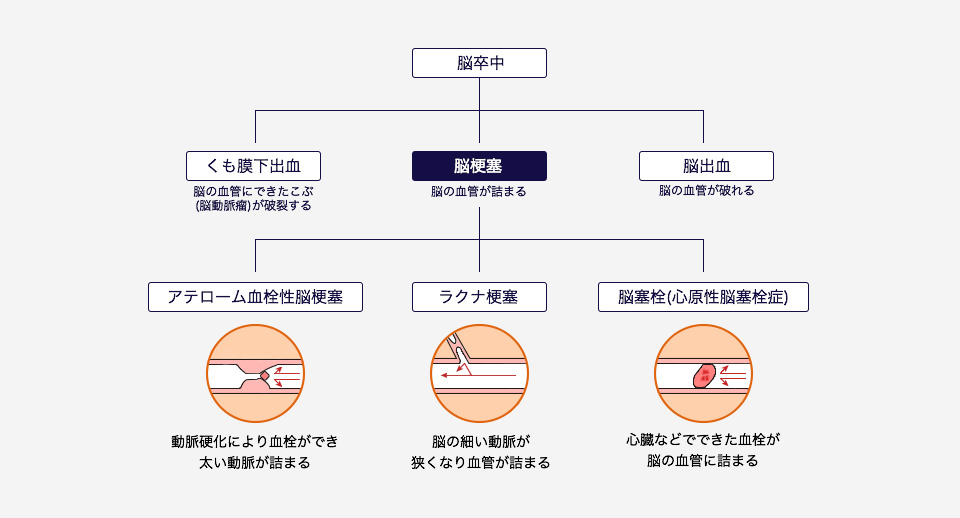
脳の血管が破れたり詰まったりして、その先の細胞に栄養が届かなくなり、脳の働きに障害が起きる疾患のことを脳卒中と言います。脳卒中は原因により、「脳の血管が詰まるタイプ(脳梗塞)」と「脳の血管が破れるタイプ(脳出血、くも膜下出血)」の大きく2つに分けられますが、70〜75%が脳梗塞だと言われています。
詰まった血管の部位により症状は異なりますが、脳梗塞をいったん発病すると、たとえ命が助かったとしても、多くの場合、麻痺や言語障害などの後遺症が残ってしまいます。
脳の血管の病気は、日本人の死亡原因の第4位であり、介護が必要になった人の18.4%は脳卒中が原因とされています。
脳梗塞の罹患者数
日本人の年間発症患者数は23〜33万人、死亡者数は年間約6万4千人、全世界での年間発症患者数は526万人超と推定されています。※1

現在の治療法
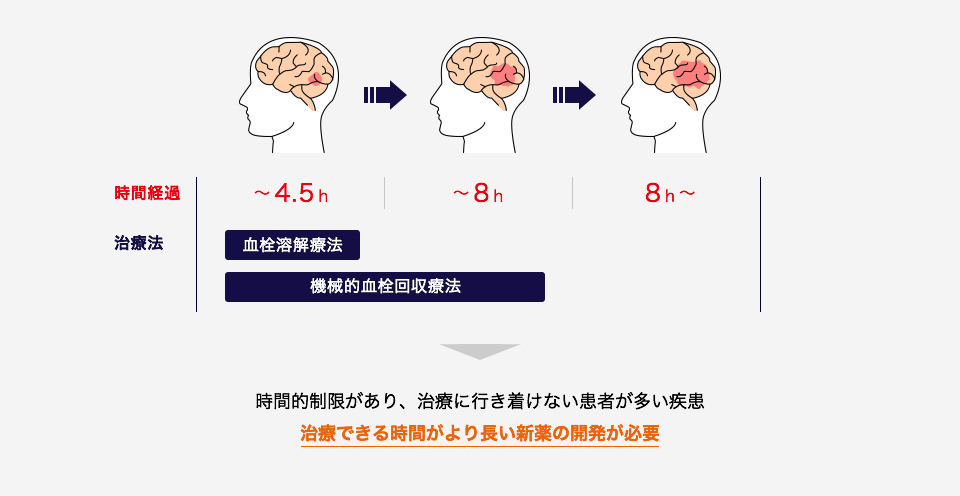
脳梗塞急性期の治療には、一般的に脳の血管に詰まった血の塊を溶かす「血栓溶解療法(t-PA治療)」や、閉塞した脳動脈内の血栓を直接回収する等で血流を再開させる「機械的血栓回収療法」が用いられますが、「血栓溶解療法」の適応は発症後4.5時間以内、「機械的血栓回収療法」でも8時間以内に限定されます。そのため脳梗塞発症後から時間が経過した後でも、治療に効果的である新薬の開発が待ち望まれています。
- ※治療は患者の状況や症状分類にて応じて実施され、「血栓溶解剤」「機械的血栓回収療法」以外の治療法も実施されています。
ヘリオスが目指す新規細胞治療法
当社は、米国Athersys, Inc.(アサシス社)が創製した幹細胞製品MultiStem®(HLCM051)について、全世界での権利を保有し、脳梗塞急性期に対する新規の細胞治療法を開発しています。
HLCM051は免疫抑制剤が不要で、静脈注射(点滴)により患者さんに投与されます。投与後は、体内へ蓄積することなく消失することが確認されています。
脳梗塞急性期に対するHLCM051の作用については、アサシス社がアメリカとイギリスで治験を実施し、患者さんに対する安全性と、一定の条件(脳梗塞を発症してから早期にHLCM051が投与された患者さん) において治療効果が期待されることが示されました。
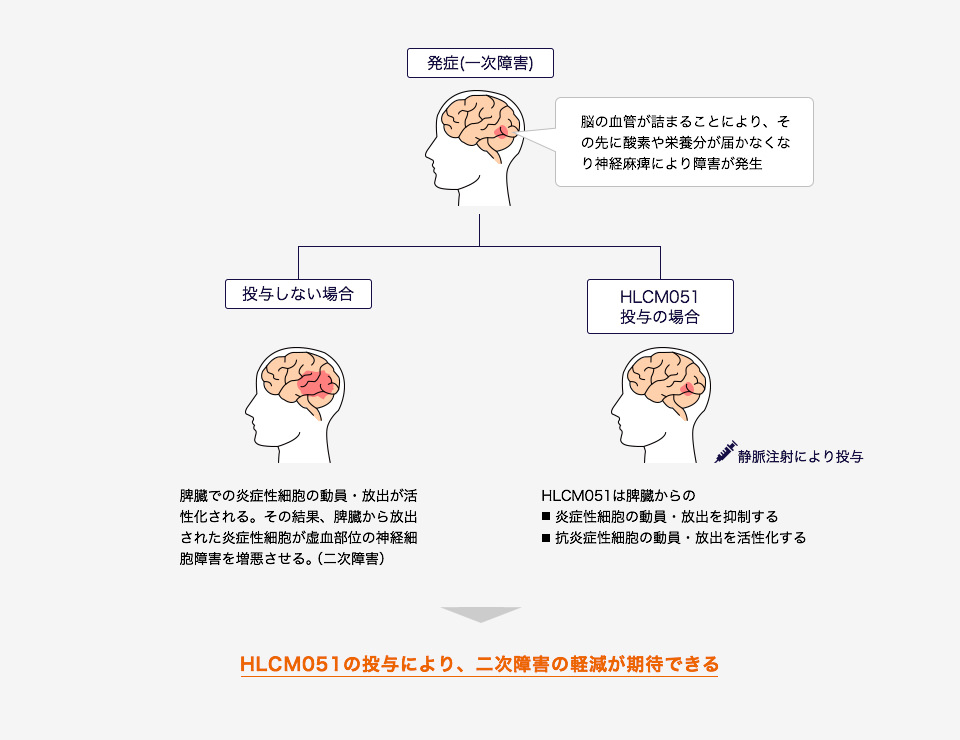
HLCM051は、免疫応答の場である脾臓(ひぞう)で炎症免疫細胞の活性化を抑制することにより、炎症や免疫反応を抑えて神経細胞の損傷を抑制、さらに、抗炎症性細胞を増殖させ、栄養因子を放出することで神経保護作用などが期待されます。
当社は現在、日本国内において脳梗塞急性期の患者さんを対象に第Ⅱ/Ⅲ相臨床試験(治験名:TREASURE試験)を実施しました。脳梗塞発症後36時間以内の患者さんに、HLCM051あるいはプラセボを静脈注射で1回投与する、というものです 。本治験の詳細は、米国国立医学図書館が管理するウェブサイトClinicalTrials.gov、及び一般財団法人医薬情報センターの管理する臨床試験情報(JapicCTI-173561)に登録・公開しています。
今後のデータの取得・申請方針について、グローバルでの治験について検討中です。
なお、HLCM051は厚生労働省より再生医療等製品として2017年2月「先駆け審査指定制度」対象品目の指定を受けています。
先駆け審査指定制度についての詳細は以下の厚生労働省のサイトをご参照ください。「先駆的医薬品指定制度」
