iPSC再生医薬品とは
iPS細胞(人工多能性幹細胞)とは、皮膚などの体細胞にいくつかの因子を導入することによって作り出される、様々な組織や臓器の細胞に分化する能力(多能性)と、ほぼ無限に増殖する能力(増殖能)を持った細胞です。
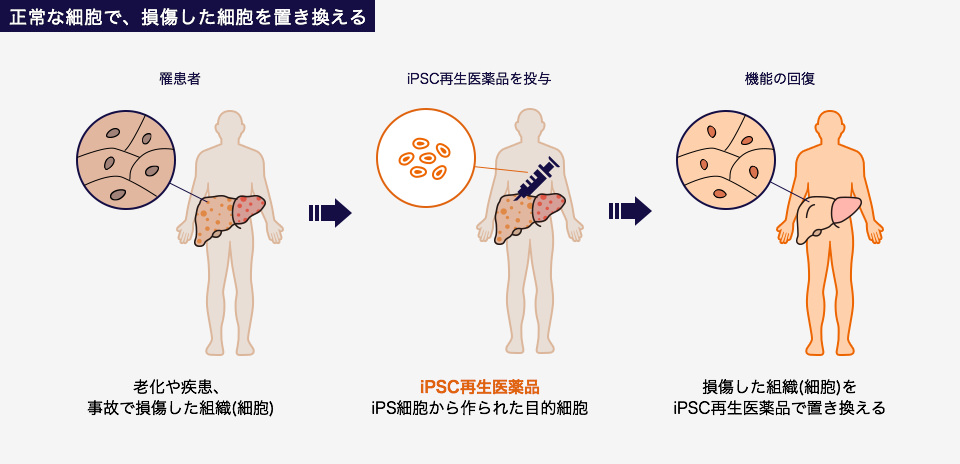
iPSC再生医薬品は、iPS細胞を分化誘導(細胞を特定の機能を持った細胞に人為的に変化させること)して人体と近似の機能を持つ細胞を作製し、その細胞を移植することによって、機能不全に陥った細胞等を置換して機能を回復することを目的とする製品です。
次世代に向けた研究活動
当社は、iPSC再生医薬品の将来の基盤技術となりうる新規技術・ノウハウをいち早く確立し、実用化を加速させるため、国内外の研究機関や企業との提携のみならず自社研究開発にも積極的に取り組んでいます。
この方針の下、遺伝子編集技術を用いたHLA型に関わりなく免疫拒絶のリスクの少ない次世代iPS細胞の作製、iPS細胞技術と遺伝子編集技術を組み合わせた次世代がん免疫細胞の作製などの研究活動を進めています。
